Biokémia
Jelentkezz be a hozzászóláshoz.
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
dixitque deus fiat lux
én legalábbis örültem neki, még akkor is ha nem feltétlenül tetszett a stílusa; de miért kéne tetsszen és miért kéne nekem? (: (költõi kérdések)
engem az állatok és gépek ötvözése bizonyos szinten érdekel.
Én úgy vagyok, hogy nem tudom elfogadni azt a tényt, hogy öregedünk (: Idegesít az a gondolat, hogy csak egy meghatározott, vagy egy meg nem határozott, de véges idõintervallum áll rendelkezésünkre, hogy megértsünk "dolgokat";
Nincsenek túlzottan speciális ismereteim a témáról, mert még az alapokat próbálom megérteni, de én úgy látom, hogy lényegében kétféleképpen lehetne megállítani/manipulálni az öregedést (és mind2 nagyon futurisztikus):
-vagy sejtszinten kéne módosítani a rendszert, hogy stacioner állapot tudjon kialakulni (telomer regeneráció, fehérje glikolizáció gátlása, stb.)
-vagy áthelyezni az egész rendszert egy olyan alapra, amely eleve irányítottan stacioner
Mind2 nagyon-nagyon távoli és még rengeteg mindent meg kell értenünk, de én ilyen irányokban szeretnék majd kutatni pár év múlva.
dixitque deus fiat lux
"Paul Root Wolpe, Ph.D., is a professor in the Department of Psychiatry at the University of Pennsylvania"
igazából ez is csupán az ism. terj. színvonalat ütné meg
valóban nem tér ki arra, h mi a GFP jelentõsége (bár sztem az ott ülõ hallgatóság nagyobb része tudja és hallott már róla épp elég elõadást, meg nem is ez volt a téma)
A vége felé még mutatott példákat az állatok és gépek "ötvözésére", távirányítású rovarok, majom, amelyik robotkart vezérel a gondolatával...
no meg tápban levõ vmilyen agy, amelyiket számításokra próbálnak felhasználni
Biztos ilyen téren levõ mûveletlenségemnek köszönhetõ, h érdekes kis összefoglalónak találtam arról, h milyen dolgokat valósítottak már meg az elmúlt években. De hát vhonnan én is kell szerezzek némi ism. terj. híreket :|
Nem hiszem, h a gonosz biomérnökökrõl lett volna szó a tudósközösség egy ilyen elõadásában. Mindenesetre a végén felvetette, h etikai kérdések is felmerülnek a jövõt illetõen.
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
ekkor kapcsoltam ki a videót.
lehet, hogy nem így akarta elõadni és én értettem félre, lehet, hogy "my bad", but I felt offended.
dixitque deus fiat lux
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
dixitque deus fiat lux
Paul Root Wolpe: It's time to question bio-engineering
Csak ezen cikkre való hivatkozásokat találtam. Próbáltam összeolvasni, h most akkor mi is van, de el kellene a segítség az értelmezésben. Az eredeti cikkhez már nem volt türelmem, csak az elõtte levõ összefoglalókhoz/hírekhez.
Azt csipegettem össze, h az ösztrogén blokkolja a caspase-12 gént, ami gátolná, csökkentené a gyulladásos immunreakciót. Majd a caspase-12-rõl meg hogy citokinokat gyárt, amik meg pont hogy az immunreakciókat serkenti (ugye, most akkor melyik?). Aztán vmi olyanról írtak, h az afrikaiaknál van olyan változata ennek a génnek, ami túl erõs reakciókat válthatnak ki (szepszis), viszont hatékonyabbak az LPS-es (Lipopoliszacharid) mikrobák ellen.
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
dixitque deus fiat lux
1ébként a kép okés, így gondoltam én is, de itt sincsen a végtermék 1ik nukleotidján sem 3 foszfátcsoport, hanem mindhez tartozik 1 (ill, mindegyik közt van egy és egyik végén +1)
de itt egy kép, ha ez által érthetõbb:

dixitque deus fiat lux
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
elképzelhetõ, hogy a méhviasz aromáját maga a viasz adja, ebben az esetben elég kicsi lehet a tenziója (egyensúlyi gõznyomása) és lehet, hogy kis koncentrációban is nagy ingert vállt ki a receptorokból, így ez megmagyarázza, hogy sokáig van intenzív illata
dixitque deus fiat lux
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
pl. a kámfor nagyon gyorsan elfogy, de ez a szublimáció miatt van, ami egy fázisátalakulás.
Sok aromaanyag folyadék halmazállapotú tisztán (pl citrullin,fahéjaldehid stb) ezeknek jóval nagyobb a tenziója, mint a szilárd anyagokénak de persze ez is anyagfüggõ.
dixitque deus fiat lux
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
dixitque deus fiat lux
Az én tudásom szerint (amit majd részletezni is fogok), a fájdalomcsillapításkor a prosztanoidok szintézisében résztvevõ cyclooxygenázt gátolja, méghozzá úgy, hogy az annak aktív centrumában lévõ szerin-t acilezi, ami in vivo irreverzibilis.
Mivel az acetil-szalicilsav igen kicsi molekula, ezért valszeg nem annyira specifikus, sok enzim aktív centrumába befér és acilezheti az enzimet
dixitque deus fiat lux
Másrészt a kémiához kapcsolódóan remélem mindenki ismeri a Vegyészoperát, ami egyedülálló 😊
A kaktusz is azért szúr, mert soha nem simogatják... Nem a remény hal meg utoljára, hanem a sejtszintű enzimműködés. n_n
Rendben, fogok írni elõször amikrõl fejbõl tudok: a cyclooxygenase inhibitorokról (pl. aszpirin) és a béta-laktám típusú antibiotikumokról (pl. penicilin-G), ha az úgy megfelel ((((:
dixitque deus fiat lux
Nagyon érdekes ez a topic. Ha megkérhetlek írnál a gyógyszerek hatásmechanizmusáról?? (pl. fájdalomcsillapítól, antibiotikumok) talán a 2. érdekelne jobban
Elóre is kössz!
azt szeretném, hogy leírjam elõször az alap dolgokat, úgy, hogy az elõismeretek nélkül is érthetõ legyen (!) és csak azután írni különlegesebb dolgokról, ami a leírt alapokra támaszkodik.
pl. így hogy írtam a DNS-rõl, már írhatok a DNS-metilációról, ami engem nagyon megfogott amikor olvastam róla
dixitque deus fiat lux
nem tudom biztosra, hogy milyen a DNS legelsõ nukleotidja bioszintéziskor, lehetséges, hogy sokkal összetettebb mechanizmusokkal indul, én csak azt próbáltam szemléltetni, ahogy a lánchosszabbítás megy és abban trifoszfátok vannak.
Ha nincs semmilyen összetettebb lépés az elején, akkor igen, indulunk egy trifoszfáttal, jön egy második trifoszfát amirõl egy difoszfát leválik és így a dinukleotidon összesen 4 foszfátcsoport lesz: 3 a legelsõ nukleotidon és 1 a kettõ között
dixitque deus fiat lux
Eleinte azt mondod, h 2 nukleozid-trifoszfát kapcsolódik össze és 1 difoszfát megy el, akkor 4foszfát csop. kéne maradjon. De utána meg "az újonnan bejövõ nukleozid-nak"-ként fogalmazol, tehát akkor az eleje csak elírás volt és a helyzet az, h már van 1 foszfátcsoportos nukleotid és ahhoz kezd csatlakozni egy trifoszfátcsoportos?
1ébként nagyon rendes tõled, h ezt így összeírod, köszi.
A DNS (Dezoxiribonukleinsav)

Hol máshol lehetne kezdeni a biokémia tárgyalását, mint a DNS-nél, ennél a csodálatosan elegáns óriásmolekulánál, amely az élet tervrajzát szolgáltatja.[/retorikai módszerek OFF]
Mindenki hallotta már, hogy a DNS-re úgy is szoktak hivatkozni, mint az örökítõanyag, genetikai információ stb., még talán az is közismert, hogy "kettõs spirál" és α-hélix. Ezeknek a fogalmaknak a megértéséhez már szükséges a molekula ismerete és a mélyebb megértéséhez (pl. hogy miért kettõs spirál) a DNS kémia tulajdonságának ismerete, amit itt be is fogok mutatni.

3 alapvetõ egységbõl épül fel a DNS, ahogy a képbõl is látszik: a lánc gerincét alkotó cukorból(piros 5szög) és foszfát csoportból((P)) (vagyis cukor-foszfát lánc), és a bázisokból(sárga sokszög)(amibõl 4-féle van).
Ez látható az alábbi képen is a négy különbözõ bázissal:
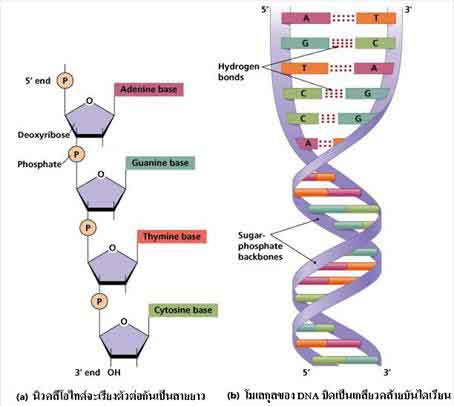
Ha kiveszünk egyetlen bázis-cukor-foszfát 3-ast, azt nukleotidnak hívjuk és kirészletezve a kémia szerkezetét ilyen:

Ezen a képen a 4 lehetséges bázis közül az adenin van lerajzolva, ezért a fent látható molekula kémiai neve adenozin-monofoszfát. Az "-ozin" jelzi számunkra, hogy a bázishoz egy cukor is kapcsolódik, valamint a "mono-" azt jelzi, hogy 1 foszfát csoport van a molekulában, ugyanis lehetne 2 (di-), vagy 3 (tri-) is (pl. Adenozin-trifoszfát)! Ilyenkor több foszfátcsoport kapcsolódik egymás után:

Amikor a DNS bioszintézise folyik (tehát az összerakása a szervezetben), akkor az mindig 3 foszfát csoportot tartalmazó nukleotidokból történik (tehát trifoszfátok). Ez azért van, mert a nukleotidok összekapcsolása (tehát a lánc építése) energiaigényes folyamat és a foszfát-csoportok összekapcsolásában "energiát lehet tárolni". Ez úgy lehetséges, hogy egy trifoszfát molekulának a foszfát kötései viszonylag kedvezõtlenek, ezért ha létezik, akkor az magas energiájú. Így érthetõ az, hogy egy trifoszfát megbontása monofoszfáttá energiát szolgáltat a DNS bioszintéziséhez.
Sõt ez annyira elterjedt, hogy a trifoszfátok (fõként az Adenozin-trifoszfát - ATP) a szervezet legfontosabb köztes-energiatároló molekulája! A legtöbb energiaigényes reakció energiáját ATP szolgáltatja (molekulák energiaigényes összerakása, molekulák energiaigényes szállítása, mozgás, beleértve az izommûködést is! stb.) és amikor a szervezetünk energiatermelõ reakciókat végez (pl glükóz lebontása), akkor az ATP formájában keletkezik, de errõl majd késõbb (:
Tehát amint írtam a DNS bioszintézise nukleozid-trifosztfátokból történik, természetesen fehérjék segítségével. Amikor két nukleozid-trifoszfát összekapcsolódik, akkor az újonnan bejövõ nukleozid-nak egy difoszfát-csoportja leválik, és a maradék foszfát-csoporton keresztül csatlakozik az elsõ nukleozid cukor részéhez(foszfodiészter kötés), így kialakítva a megszokott cukor-foszfát gerincet:
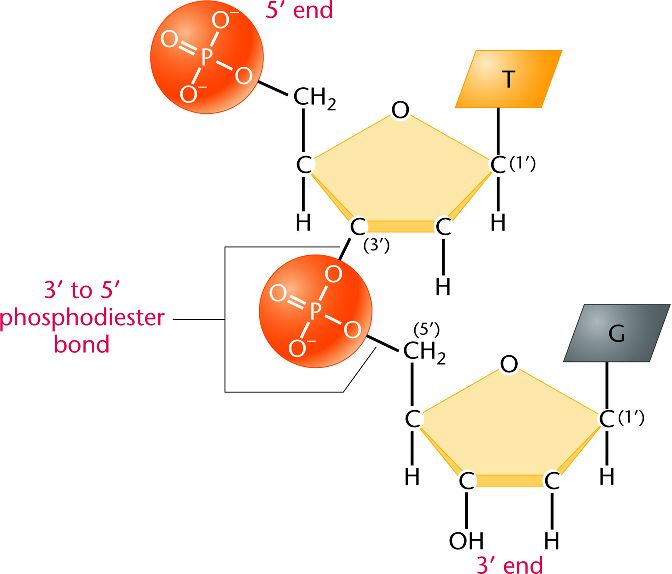
A képen is fel van tüntetve a foszfátcsoport maradék negatív töltése, amely nagyon fontos szerepet tölt be a DNS szerkezetét illetõen.
Nagyon fontos megérteni a hidrofobicitás/hidrofilitás fogalmát, mert nagymértékben befolyásolja a makromolekulák (pl DNS, fehérjék) térszerkezetét!
Közismert, hogy vannak olyan anyagok, amelyek nem oldódnak vízben (hidrofóbok; hydros-víz, phobosz-félni), pl az olaj, míg mások igen, pl a konyhasó (nátrium-klorid, NaCl) (hidrofilek; -philia, szeretni).
Az oldódás annyit jelent, hogy az oldószer molekulái (pl. víz) körbeveszik (szolvatálják, kialakul egy szolvát burok) az oldandó anyag molekuláit. Ez persze nem véletlenül történik, hanem termodinamikai hajtóereje van és csak akkor történik meg, ha a szolvatáció energianyereséggel jár.
Ehhez tudnunk kell a víz szerkezetérõl, hogy egy ún. dipólusú molekula:
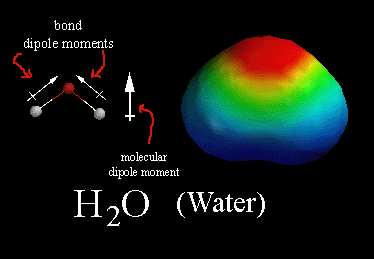
Ez annyit jelent, hogy a molekulában az elektronok nem egyenletesen oszlanak el, jelen esetben az oxigén atom felé vannak eltolva, ahogy az az elektrosztatikus potenciál képbõl is látszik (piros~nagy elektronsûrûség, kék~kicsi). Ez azért van, mert az oxigén atomnak nagyobb az elektronegativitás értéke, ami az atom szerkezetének a következménye. Képletesen szólva az oxigén magára húzza az O-H kötésben résztvevõ elektronpárt, így az oxigénen nagyobb az elektronsûrûség, ami õt picit negatívabba (δ-), míg a hidrogéneket kicsit pozitívabbá (δ+) teszi.
Ennek köszönhetõen a vízmolekulák egymással ilyen ún. másodlagos kölcsönhatásokkal kapcsolódnak (dipol-dipol kölcsönhatás), ráadásul a víz molekula oxigén δ- atomja és a másik víz δ+ hidrogénje között olyan erõs kölcsönhatás lép fel, hogy az oxigén kicsit "magára húzza" a szomszédos víz hidrogénjét (hidrogén hidas kölcsönhatás)
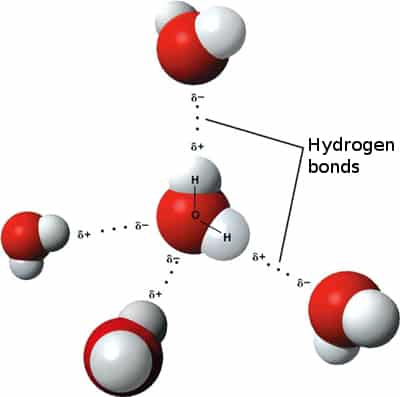
A másodlagos kölcsönhatások csökkentik a rendszer energiáját, mert valamelyest semlegesítik egymást a kialakuló részleges töltések.
Visszakanyarodva az oldódáshoz, a NaCl egy ionos vegyület, ami azt jelenti, hogy kationokból és anionokból áll, szilárd formában még ionrácsban, amit a kilakult +/- töltések tartanak össze. Ha egy NaCl kristályt vízbe dobunk, akkor a töltéssel rendelkezõ kationokat és anionokat a dipólus H2O molekulák szolvatálni tudják, hiszen õk rendelkeznek parciális töltéssel (δ+/-), így az anyag oldódik:


dixitque deus fiat lux
Kicsit trükkösebb a helyzet, ha egy olyan molekulánk van, aminek van hidrofób és hidrofil része is! Ilyenek a foszfolipidek, amelyek egy poláros feji részbõl (foszfát-csoport) és egy apoláros farki részbõl (hosszú szénláncú zsírsav) állnak:
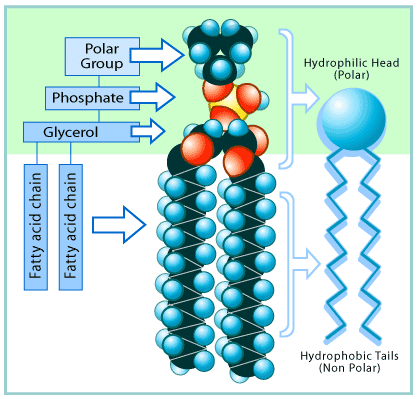
Ilyenek anyagokat vízbe rakva úgy rendezõdnek molekuláris szinten, hogy a poláris hidrofil rész a vízzel, míg az apoláros hidrofób rész más apoláris részekkel érintkezzen. Ez teszi lehetõvé micellák és membránok létrejöttét:

És végül amiért ebbe az egészbe belekezdtem 😄
A DNS gerincét alkotó cukor-foszfát lánc poláris jellegû fõként a meglévõ negatív töltés és részlegesen a cukron lévõ, vízhez hasonló OH- csoportok miatt, míg ha a bázisokat szemrevételezzük, akkor azok fõként apolárisak, hidrofóbok. Ezért a DNS kettõs-spirál a térben úgy rendezõdik, hogy a ként láncon lévõ bázisok befele, egymással szemben -létraszerûen- helyezkednek, míg a poláris, hidrofil rész kívül van. A DNS spirális formát vesz fel, hogy minél kevésbé érintkezzenek a hidrofób bázisok vízzel.
Az így kialakult képünket a DNS-rõl még annyiban szeretném módosítani, hogy végre pontosan megnevezem a bázisokat, íme:


A,T,G,C - adenin, timin, guanin, citozin. Ez a négy bázis építi fel a DNS-t és ezeknek a sorrendje határozza meg a genetikai információt. Kettõs spirál révén, mindig két bázis van egymással szemben (bázispárosodás), mindkét szálon 1-1 nukleotidonként, így alakítva ki a létraszerû elrendezõdést. Még a hélix szerkezetének felfedezése elõtt észrevették, hogy A-ból mindig ugyanannyi van, mint T-bõl és G-bõl, mint C-bõl, ezt elnevezték Chargaff féle bázispárosodási szabálynak. Csak a szerkezet megfejtése után derült ki, hogy mindez azért van, mert párosodáskor A-val szemben mindig T van és G-vel szemben mindig C (és vica-versa). Ennek oka az, hogy a bázisok így összekapcsolódva "egymás komplementerei", a két komplementer bázis között így alakulnak ki a legerõsebb másodlagos kötések, amik stabilizálják a kettõs hélixet.
dixitque deus fiat lux
terveim közt szerepel hamarosan írni ide a topikba az alapfogalmakról, hogy mindenki érthesse, akit érdekel a téma, és utána belemenni speciálisabb témákba (pl. a HIV-proteáz, retrovírusok)
csak nagyon kevés idõm van az egyetem miatt.
talán hétvége körül írok a DNS-rõl részletesen és talán a fehérjékrõl, csak bazi nagy anyag ((:
dixitque deus fiat lux
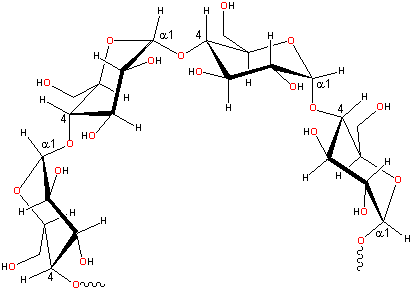
Van olyan poliszacharid, ami csak β-glükózt tartalmaz, ez a cellulóz:
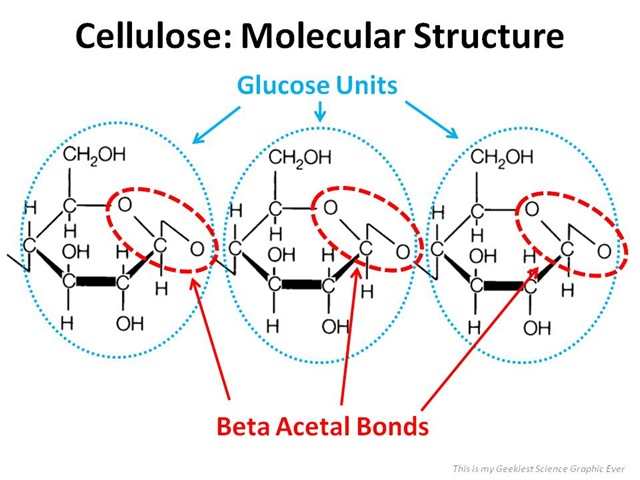
és ennek az az érdekessége h a cellulóz jóval ellenállóbb, mint a keményítõ. pl a cellulózt nem is tudja az ember lebontani...de vajon miért? 😛
dixitque deus fiat lux
Ha van 100 db D-glükóz molekulád kristályban, akkor az nyílt láncban van, és így néz ki:

Viszont ha most ezt a 100 molekulát vízbe rakod, akkor gyûrûbe fog záródni (ez a laktonizáció), és a gyûrûnek két állása képzelhetõ el:


Ez az α,β-glükóz, pontosabban α,β glükopiranóz (ez a piranóz gyûrû). A két forma egymásba át tud alakulni oldatban, ezt hívják mutarotációnak és abból a formából lesz több, amelyik stabilabb, jelen esetben α:β 36:64 és ez azért van, mert β állásban a nagy térigényû OH- csoport a legtávolabb van a gyûrûtõl, így minimalizálódik a taszítás.
dixitque deus fiat lux
Ha létezik egy olyan molekula, amelyikben van 1 királis C-atom (tehát annak a molekulának létezik tükörképi párja, ezt úgy hívják, hogy enantiomerje) akkor az a polarizált fény síkját valamerre forgatja (+)/(-).
Ha egy királis molekula a polarizált fényt (+)-ba forgatja, akkor annak a tükörképi párja (enantiomerje) (-)-ba fog forgatni.
Ha összeöntöd a két molekulát, és mindkét molekulából ugyanannyi van az elegyben, akkor az már nem fog forgatni (ezt racém elegynek hívják), mert amennyit az egyik molekula (+)-ba forgat, annyit forgat a másik (-)-ba.
dixitque deus fiat lux
