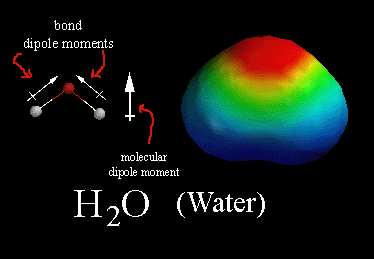Biokémia és más interdiszciplináris tudományok
-
 #18
#18
Szeretném bemutatni az alapvető biomolekulákat és ezen keresztül egy alapvető hozzáállást szemléltetni, mely szvsz szükséges a biokémiai rendszerek (annak mechanizmusai, tulajdonságai stb.) megértéséhez. Ez egy elég nehéz feladat, mert az ember alapvetően úgy sajátítja el, hogy huzamosabb időn keresztül ezzel foglalkozik és kifejlődik benne ez a speciális "intelligencia", amit elég nehéz így átadni ... mindenesetre én próbálkozom (:
A DNS (Dezoxiribonukleinsav)
Hol máshol lehetne kezdeni a biokémia tárgyalását, mint a DNS-nél, ennél a csodálatosan elegáns óriásmolekulánál, amely az élet tervrajzát szolgáltatja.[/retorikai módszerek OFF]
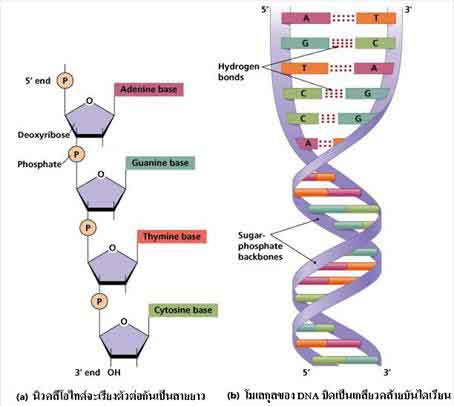
Mindenki hallotta már, hogy a DNS-re úgy is szoktak hivatkozni, mint az örökítőanyag, genetikai információ stb., még talán az is közismert, hogy "kettős spirál" és α-hélix. Ezeknek a fogalmaknak a megértéséhez már szükséges a molekula ismerete és a mélyebb megértéséhez (pl. hogy miért kettős spirál) a DNS kémia tulajdonságának ismerete, amit itt be is fogok mutatni.
3 alapvető egységből épül fel a DNS, ahogy a képből is látszik: a lánc gerincét alkotó cukorból(piros 5szög) és foszfát csoportból((P)) (vagyis cukor-foszfát lánc), és a bázisokból(sárga sokszög)(amiből 4-féle van).
Ez látható az alábbi képen is a négy különböző bázissal:
Ha kiveszünk egyetlen bázis-cukor-foszfát 3-ast, azt nukleotidnak hívjuk és kirészletezve a kémia szerkezetét ilyen:
Ezen a képen a 4 lehetséges bázis közül az adenin van lerajzolva, ezért a fent látható molekula kémiai neve adenozin-monofoszfát. Az "-ozin" jelzi számunkra, hogy a bázishoz egy cukor is kapcsolódik, valamint a "mono-" azt jelzi, hogy 1 foszfát csoport van a molekulában, ugyanis lehetne 2 (di-), vagy 3 (tri-) is (pl. Adenozin-trifoszfát)! Ilyenkor több foszfátcsoport kapcsolódik egymás után:
Amikor a DNS bioszintézise folyik (tehát az összerakása a szervezetben), akkor az mindig 3 foszfát csoportot tartalmazó nukleotidokból történik (tehát trifoszfátok). Ez azért van, mert a nukleotidok összekapcsolása (tehát a lánc építése) energiaigényes folyamat és a foszfát-csoportok összekapcsolásában "energiát lehet tárolni". Ez úgy lehetséges, hogy egy trifoszfát molekulának a foszfát kötései viszonylag kedvezőtlenek, ezért ha létezik, akkor az magas energiájú. Így érthető az, hogy egy trifoszfát megbontása monofoszfáttá energiát szolgáltat a DNS bioszintéziséhez.
Sőt ez annyira elterjedt, hogy a trifoszfátok (főként az Adenozin-trifoszfát - ATP) a szervezet legfontosabb köztes-energiatároló molekulája! A legtöbb energiaigényes reakció energiáját ATP szolgáltatja (molekulák energiaigényes összerakása, molekulák energiaigényes szállítása, mozgás, beleértve az izomműködést is! stb.) és amikor a szervezetünk energiatermelő reakciókat végez (pl glükóz lebontása), akkor az ATP formájában keletkezik, de erről majd később (:
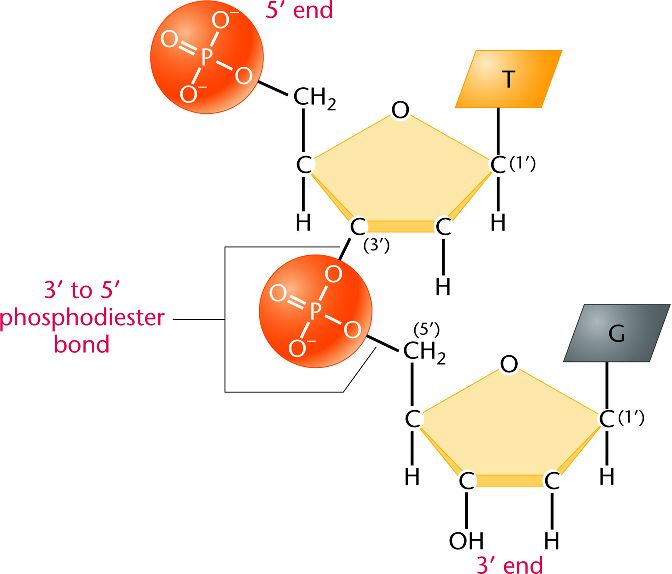
Tehát amint írtam a DNS bioszintézise nukleozid-trifosztfátokból történik, természetesen fehérjék segítségével. Amikor két nukleozid-trifoszfát összekapcsolódik, akkor az újonnan bejövő nukleozid-nak egy difoszfát-csoportja leválik, és a maradék foszfát-csoporton keresztül csatlakozik az első nukleozid cukor részéhez(foszfodiészter kötés), így kialakítva a megszokott cukor-foszfát gerincet:
A képen is fel van tüntetve a foszfátcsoport maradék negatív töltése, amely nagyon fontos szerepet tölt be a DNS szerkezetét illetően.
Nagyon fontos megérteni a hidrofobicitás/hidrofilitás fogalmát, mert nagymértékben befolyásolja a makromolekulák (pl DNS, fehérjék) térszerkezetét!
Közismert, hogy vannak olyan anyagok, amelyek nem oldódnak vízben (hidrofóbok; hydros-víz, phobosz-félni), pl az olaj, míg mások igen, pl a konyhasó (nátrium-klorid, NaCl) (hidrofilek; -philia, szeretni).
Az oldódás annyit jelent, hogy az oldószer molekulái (pl. víz) körbeveszik (szolvatálják, kialakul egy szolvát burok) az oldandó anyag molekuláit. Ez persze nem véletlenül történik, hanem termodinamikai hajtóereje van és csak akkor történik meg, ha a szolvatáció energianyereséggel jár.
Ehhez tudnunk kell a víz szerkezetéről, hogy egy ún. dipólusú molekula:
Ez annyit jelent, hogy a molekulában az elektronok nem egyenletesen oszlanak el, jelen esetben az oxigén atom felé vannak eltolva, ahogy az az elektrosztatikus potenciál képből is látszik (piros~nagy elektronsűrűség, kék~kicsi). Ez azért van, mert az oxigén atomnak nagyobb az elektronegativitás értéke, ami az atom szerkezetének a következménye. Képletesen szólva az oxigén magára húzza az O-H kötésben résztvevő elektronpárt, így az oxigénen nagyobb az elektronsűrűség, ami őt picit negatívabba (δ-), míg a hidrogéneket kicsit pozitívabbá (δ+) teszi.
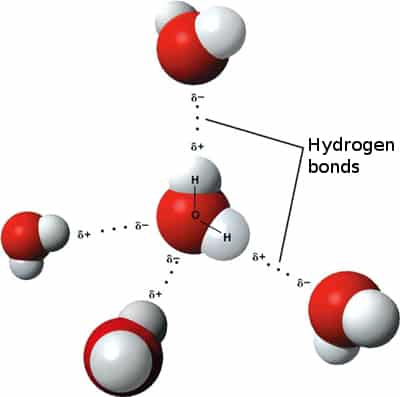
Ennek köszönhetően a vízmolekulák egymással ilyen ún. másodlagos kölcsönhatásokkal kapcsolódnak (dipol-dipol kölcsönhatás), ráadásul a víz molekula oxigén δ- atomja és a másik víz δ+ hidrogénje között olyan erős kölcsönhatás lép fel, hogy az oxigén kicsit "magára húzza" a szomszédos víz hidrogénjét (hidrogén hidas kölcsönhatás)
A másodlagos kölcsönhatások csökkentik a rendszer energiáját, mert valamelyest semlegesítik egymást a kialakuló részleges töltések.
Visszakanyarodva az oldódáshoz, a NaCl egy ionos vegyület, ami azt jelenti, hogy kationokból és anionokból áll, szilárd formában még ionrácsban, amit a kilakult +/- töltések tartanak össze. Ha egy NaCl kristályt vízbe dobunk, akkor a töltéssel rendelkező kationokat és anionokat a dipólus H2O molekulák szolvatálni tudják, hiszen ők rendelkeznek parciális töltéssel (δ+/-), így az anyag oldódik:
[FOLYTATÁS A #17-ben]